Goed, we mogen dus deelnemen. Oké, wat behelst dat onderzoek dan precies? Het behelst de QRL 201-studie van het bedrijf Quralis (ik neem aan dat het een woordspeling is op Cure ALS, hetgeen ik hoop dat ze lukt). Het is een fase 1-onderzoek, wat wil zeggen dat het een experimenteel onderzoek is, slechts 16 man gingen mij voor. Ze testen welke dosering van deze medicatie nodig is om genoeg van het werkzame spul in mijn lichaam te krijgen. Het onderzoek bestaat uit een groep van 40 mensen. Een kwart daarvan zit in en placebo-groep. De medicatie wordt toegediend via een ruggenprik, zodat het spul direct in je hersenvocht komt. Je krijgt vijf van die doseringen over drie maanden tijd. En vervolgens gaan ze controleren wat het effect is.
Wat doet de medicatie? Ik zal proberen het hier in mijn woorden uit te leggen wat ik geleerd heb door te lezen en te spreken met medewerkers. Eerst een stukje biologie.
Probleem
Er lopen lange kabels van cellen (zenuwuitloper) van je hersensen tot je spieren. Deze vervoeren de berichten van je hersenen om iets te bewegen, naar je spieren. Deze cellen groeien niet meer bij al je eenmaal volwassen bent. Daarom onderhoudt het lichaam ze goed. Dat doet het Stathmin-2 eiwit.

De bouwinstructies van alle verschillende soorten eiwitten zitten gecodeerd in je DNA. Eiwitten worden geproduceerd in de eiwitfabrieken die in je cellen aanwezig zijn. Wanneer er een nieuw eiwit gemaakt moet worden, kopieert een RNA-molecuul het relevante deel van het DNA dat die bouwinstructies bevat, en verplaatst zichzelf dan naar de eiwitfabriek. Met als eindresultaat een eiwit.
Wat ze te weten zijn gekomen, is dat een eiwit TDP-43 zich opstapelt buiten de celkern bij 95% van de patiënten met ALS (waarom is niet helder). Op het moment dat het daar is, is het toxisch voor de productie van andere eiwitten. De belangrijkste daarvan zijn het Stathmin-2 en het UNC13A eiwit.
Relevant voor deze studie is het Stathmin-2 eiwit waar ik het net over had (dat eiwit dat je zenuwkabels onderhoudt). De ophoping van TDP-43 buiten de celkern zorgt ervoor dat de RNA-splitsing van eiwit Stathmin-2 niet goed werkt. Met als gevolg geen correct Stathmin-2 eiwit.
Omdat er uiteindelijk te weinig van die Stathmin-2’s eiwitten zijn, beginnen de zenuwkabels af te sterven. En daardoor ervaar ik verminderde kracht.
Oplossing
Het medicijn dat ze injecteren in mijn hersenvocht bevat een zogenaamde ASO, een Antisense Oligonucleotide. Dit ASO is als een puzzelstuk dat past op het RNA-molecuul dat gebruikt wordt voor de productie van het Stathmin-2 eiwit. Het haakt eraan vast, en corrigeert dan de originele werking. Zie deze illustratie:
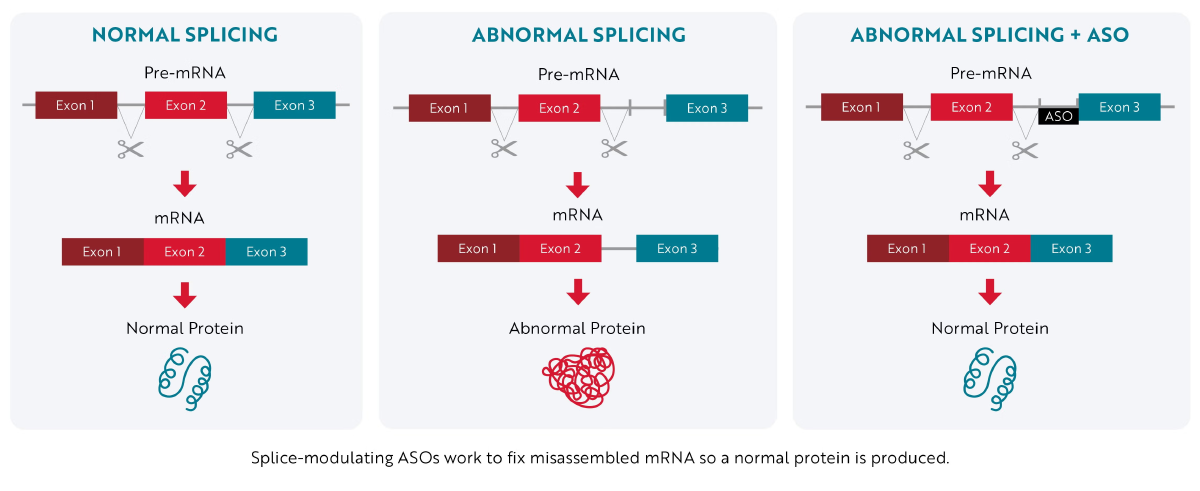
Daarmee zou, ondanks dat er een hoop toxisch materiaal buiten de celkern zit, de productie van het Stathmnin-2 eiwit toch door moeten gaan. Met als gevolg dat de reparateurs van mijn zenuwkabels er weer bij komen, en de zenuwkabels die er zijn behouden blijven.
De hoop is dat dit medicijn een vertraging of een stilstand kan betekenen in de achteruitgang van je spieren.
Het is overigens zo dat deze biologische processen niet dagen duurden, maar eerder weken of maanden, waardoor het mogelijk best wel even kan duren voor je verschil merkt.
Disclaimer
Voor alle duidelijkheid: het is geen geneesmiddel. Aangedane schade kan niet hersteld worden!
Daarnaast is het zo dat dit alleen dit specifieke Stathmin-2 eiwit corrigeert; terwijl er dus ook andere eiwitten zijn die alsnog niet meer gemaakt worden (b.v. het eerder genoemde UNC13A, waar overigens ook een experimentele studie voor komt) door die toxische ophoping die er nog altijd is, en ook tot probleme kunnen leiden.
Hoe dan ook: een hoopgevend stukje innovatie waar ik graag aan mee doe.